Marknadsnyheter
Delårsrapport för perioden 2023.01.01 – 2023.03.31
Delårsrapport för perioden 2023.01.01 – 2023.03.31
PolarCool AB (publ) publicerar delårsrapporten för första kvartalet. Hela rapporten finns tillgänglig på bolagets hemsida (https://www.polarcool.se). Nedan presenteras en sammanfattning av delårsrapporten.
Väsentliga händelser under första kvartalet
PolarCool offentliggör antalet uthyrda system 2022 samt utsikter för 2023
Bolaget meddelar att den installerade basen har ökat till 38 PolarCap® Systems i Europa. Bedömningen är att uthyrningen kommer att fortsätta öka och i slutet av 2023 uppgå till 100-150 system.
PolarCool utökar sin närvaro i tysk ishockey
Bolaget tecknar ett 2-årigt avtal med den professionellla klubben Dresdner Eislöwen för användandet av PolarCap® System.
PolarCool tar hem första avtalet i Norge – Vålerenga Hockey
PolarCool fortsätter etablera PolarCap® System inom europeisk toppishockey där norska storklubben Vålerenga Ishockey blir nästa lag att implementera PolarCap® i sina rutiner för att behandla hjärnskakningar.
PolarCool tar hem första avtalet i Danmark
Bolaget tecknar avtal med danska toppklubben Sønderjyske som spelar i danska högstaligan – Metal Ligaen.
PolarCool deltar i UEFA Medical Symposium i Frankfurt som officiell guldpartner
PolarCool deltar som en av 14 utvalda externa partners på det åttonde UEFA Medical Symposium i Frankfurt tillsammans med mer än 250 av fotbollens ledande läkare.
Styrelsen i PolarCool beslutar om en företrädesemission om cirka 7,4 MSEK – säkerställd till cirka 90 procent
Bolaget har beslutat om en företrädesemission som vid full teckning tillför Bolaget cirka 7,4 MSEK före emissionskostnader.
PolarCool tar hem ytterligare rugbyavtal med fransk Top 14-gigant
Bolaget fortsätter etablera PolarCap® System i den franska högstaligan Top 14 där Lyon Olympique Universitaire (LOU) tecknar ett tvåårigt avtal.
PolarCool växer i HockeyAllsvenskan – ligaettan MoDo Hockey tecknar avtal
Framgångarna på den svenska ishockeymarknaden fortsätter för Bolaget. HockeyAllsvenskans ligaetta, MoDo Hockey blir nästa lag att börja tillhandahålla PolarCap® System genom ett tvåårigt avtal.
Schweiziska hockeyklubben SC Bern tecknar ett 2-årigt avtal för användandet av PolarCap® System
Etableringen av PolarCap® inom schweizisk hockey fortsätter där klubbjätten SC Bern blir andra laget efter HC Davos att inkludera PolarCap® System i sin behandlingsrutin för hjärnskakningar.
Lyckad emission i PolarCool – tillförs 7,4 MSEK
Utfallet i företrädesemissionen meddelas där Bolaget tillförs cirka 7,4 MSEK före emissionskostnader (som beräknas uppgå till cirka 1,6 MSEK).
PolarCool beslutar om riktad nyemission upp till 1,5 MSEK
Styrelsen i PolarCool beslutar med stöd av bemyndigandet beviljat av extra bolagsstämma den 13 mars 2023, om en riktad nyemssion upp till 1,5 MSEK.
PolarCool meddelar utfall i den riktade nyemissionen
Styrelsen i PolarCool meddelar utfallet i den riktade emission av aktier till garanterna i den tidigare genomförda företrädesemissionen. Totalt tecknades en emissionslikvid om ca 1,3 MSEK, varav 0,3 MSEK betalas genom kvittning enligt 13 kap. 41 § aktiebolagslagen mot fordran på garantiersättning från företrädesemissionen.
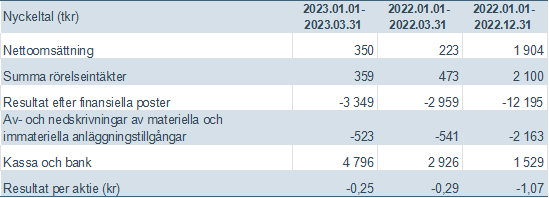
Finansiell översikt och nyckeltal

VD Erik Andersson kommenterar kvartalet
PolarCools vision är att etablera PolarCap® System som den givna akuta behandlingen av hjärnskakning. Vi vill förändra nuvarande praxis gällande akut behandling, eller om vi ska vara ärliga: brist på behandling.
Att genomföra detta är ett långsiktigt och tidskrävande arbete. Under det första kvartalet 2023 har vi fortsatt att göra marknads- och verksamhetsmässiga framsteg. Vi har stärkt vår närvaro på den europeiska marknaden genom nya avtal på både befintliga och nya marknader. Ytterligare europeiska storlag har tecknat avtal och vi har tagit betydande steg framåt i arbetet med certifieringen av vårt eget kvalitetssystem. Vi ser nu fram emot att fortsätta arbetet med att etablera PolarCap® System som en akut behandlingsmetod för hjärnskakningar.
Framgångarna i Frankrike fortsätter
Framgångarna i Frankrike fortsatte, rugbylaget Lyon Olympique Universitaire (LOU) blev nästa Top 14-lag att teckna avtal för användandet av PolarCap® System. PolarCool har på senare tid tecknat ett antal strategiska avtal med professionella rugbyklubbar i både Frankrike och Storbritannien. Vi har sedan tidigare två franska rugbyavtal med Top 14-lagkollegorna Stade Français och Racing 92. Målsättningen i närtid är att teckna fler avtal både i högstaligan Top 14 och i den franska andraligan Pro D2. För varje individuellt avtal närmar vi oss den långsiktiga målsättningen – en ligalösning.
Genombrott i Norge och Danmark
Bolaget fortsätter att etablera PolarCap® System inom nordisk toppishockey genom att ta hem första avtalen i Norge och Danmark där storklubbarna Vålerenga Hockey och Sønderjyske blir först ut. Vålerenga Ishockey är en av de mest framgångsrika klubbarna inom norsk hockey med 30 ligatitlar och danska Sønderjyske deltog så sent som säsongen 2021/2022 i Champions Hockey League. Vår förhoppning är att avtalen ska ge ökad uppmärksamhet för vår behandlingsmetod och att fler lag i respektive liga ska följa efter till nästa säsong.
Hockeygiganten SC Bern tecknar avtal
Under det första kvartalet tecknade Bolaget ett strategiskt viktigt avtal med den schweiziska ishockeyjätten SC Bern för användning av PolarCap® System. Avtalet är viktigt för Bolagets fortsatta etablering på den schweiziska marknaden där SC Bern nu blir det andra laget efter HC Davos att inkludera behandling med PolarCap® System i sina rutiner för hjärnskakningar.
Trenden håller i sig – ökad nettoomsättning jämfört med samma period 2022
Med ett ökat antal avtal fortsätter trenden med en ökad nettoomsättning. Våra avtalsintäkter periodiseras under hela avtalsperioden. Givet en förbättrad försäljning under 2022 ökade nettoomsättningen till 0,3 MSEK (0,2 MSEK) under första kvartalet 2023.
Merparten av de avtal som tecknats under Q1 2023 kommer att börja påverka nettoomsättningen under andra halvan av 2023 i samband med säsongstarterna.
Den lyckade emissionen stärker PolarCools finansiella ställning
Det positiva utfallet från företrädesemission var en mycket viktig händelse under det första kvartalet. Vi gläds åt intresset och tron på Bolaget och vi arbetar nu intensivt för att öka vår kundbas och omsättning. I och med återbetalningen av konvertibellånet i maj blir våra försäljningsframgångar än mer viktiga för Bolagets finansiella ställning.
Framsteg i MDR-certifieringsprocessen
PolarCool arbetar för att erhålla certifiering för Bolagets eget kvalitetssystem. Idag genomförs kvalitetssäkringen i samarbete med BrainCool AB (publ). I den pågående processen med att erhålla ett eget certifikat för detta enligt EU:s nya regelverk Medical Device Regulation (MDR), har vi genomfört och klarat den första revisionen av Intertek, som är en s.k. Notified Body (NB). Detta är den första av två planerade revisioner i den pågående certifieringsprocessen. Den avslutande revisionen, stage 2 audit, är planerad att ske under mitten av juni 2023. Detta är det sista steget för att PolarCool ska kunna erhålla ett eget MDR-certifikat, vilket är en viktig milstolpe och kommer innebära betydligt lägre kostnader framöver för Bolaget. Arbetet med detta kommer därför prioriteras och därmed ta betydande resurser i anspråk fram till det förväntade godkännandet under Q3.
Sammanfattningsvis så är jag nöjd med de framsteg som vi gjort hittills. Under perioden har merparten av våra kunder varit i slutet av sina säsonger och trots det har vi kunnat sluta nya avtal. När uppstarten av de nya tävlingssäsongerna nu sker under Q2 väntar en intensiv och viktig period för PolarCool inför den andra halvan av 2023. Vi har idag ett betydande antal kunddialoger vilket är en förutsättning för att nå vår målsättning för 2023.
För mer information
Erik Andersson – VD PolarCool AB (publ)
+46 – 738 60 57 00
E-mail: erik.andersson@polarcool.se
Denna information är sådan information som PolarCool AB är skyldigt att offentliggöra enligt EU:s marknadsmissbruksförordning. Informationen lämnades, genom ovanstående kontaktpersons försorg, för offentliggörande den 26 maj 2023 kl. 10.00 CET.
Hela kvartalsrapporten finns tillgänglig på bolagets hemsida (https://www.polarcool.se) och som bilaga i detta pressmeddelande.
Om PolarCool AB (publ)
PolarCool AB (publ) är ett medicinteknikföretag som utvecklar, marknadsför och säljer produkter inom idrottsmedicin. Bolaget fokuserar på behandling av hjärnskakning och upprepade huvudsmällar. PolarCool AB (publ) har sitt säte i Lund. Aktien är noterad på Spotlight Stock Market.
Marknadsnyheter
Regeringen föreslår lättnader i byggkraven för studentbostäder
Regeringen har beslutat om en lagrådsremiss med förslag till lättnader i byggkraven för studentbostäder. Syftet är att öka möjligheterna till flexibilitet vid byggandet.
– På många studieorter är det svårt för studenter att hitta boende. Därför behöver byggregelverket förenklas. Syftet är att möjliggöra för fler studentbostäder genom sänkta byggkostnader och ökad flexibilitet, säger infrastruktur- och bostadsminister Andreas Carlson.
Förslaget innebär att det blir möjligt att göra undantag från kraven på tillgänglighet och användbarhet i en byggnad som innehåller studentbostäder. Undantagen ska kunna tillämpas vid både nyproduktion och vid ändring av en byggnad.
Det ska vara möjligt att göra undantag för högst 80 procent av studentbostäderna i ett byggprojekt. Minst 20 procent av studentbostäderna ska fortfarande uppfylla gällande krav på tillgänglighet och användbarhet för personer med nedsatt rörelse- eller orienteringsförmåga.
Lagändringen ger större flexibilitet vid byggande av studentbostäder och skapar fler tänkbara sätt att utforma planlösningar. Till exempel kan bostadsytan minskas och fler bostäder rymmas inom en given yta.
De föreslagna undantagen ska inte hindra personer med funktionsnedsättning att vara delaktiga i sociala sammanhang. En studentbostad som omfattas av undantagen ska kunna besökas av en person med nedsatt rörelse- eller orienteringsförmåga.
Regeringen breddar också definitionen av studentbostäder till att inkludera all vuxenutbildning för att göra det möjligt för fler kommuner att erbjuda studentbostäder.
Förslagen föreslås träda i kraft den 1 juli 2025.
Lagrådsremissen: Lättnader i byggkraven för studentbostäder – Regeringen.se
Presskontakt
Ebba Gustavsson
Pressekreterare hos infrastruktur- och bostadsminister Andreas Carlson
Telefon (växel) 08-405 10 00
Mobil 076-12 70 488
ebba.gustavsson@regeringskansliet.se
Marknadsnyheter
Bönor från egen kaffeskog, sump till jord – Viking Lines nya kaffe gör gott på många olika sätt


Viking Lines resenärer dricker varje år 8,5 miljoner koppar kaffe. Nu satsar rederiet på ett helt nytt kaffe som ger minskade klimatutsläpp och bättre levnadsvillkor för odlarna. Kaffet från Slow Forest odlas på rederiets egen odling i Laos utan kemiska gödningsmedel, handplockas och rostas därefter i Danmark.
Allt kaffe som serveras på Viking Lines fartyg är nu hållbart producerat Slow Forest-kaffe, odlat på rederiets 75 hektar stora odling på högplatåerna i Laos och rostat i Danmark. Kaffeplantorna odlas bland träd på återbeskogad mark, i stället för på traditionellt skövlade plantager. Viking Lines odling ligger i en kolsänka där målsättningen är att plantera 30 000 träd, vilket innebär nästan 400 träd per hektar. Kaffeskogen förbättrar också den lokala biologiska mångfalden i området.
Odlingen, bearbetningen och rostningen av kaffet hanteras av Slow Forest Coffee. För företaget är det viktigt att produktionskedjan är rättvis och transparent. Utöver miljöfördelarna erbjuder Slow Forest bättre lönevillkor och sjukersättning för byns odlare.
”Den traditionella kaffetillverkningens koldioxidavtryck är stort och merparten av intäkterna går till Europa i stället för produktionsländerna. Vi ville göra annorlunda. Våra kunder vill göra hållbara val, och nu kan de njuta av sitt kaffe med bättre samvete än någonsin tidigare,” berättar Viking Lines restaurangchef Janne Lindholm.
Bönorna till Slow Forest-kaffet får sakta mogna i skuggan av träden, utan kemiska gödningsmedel. De plockas också för hand, vilket avsevärt förbättrar kaffets kvalitet och smak. Viking Lines nya kaffe består till 100 procent av Arabica-bönor, med en balanserad syrlighet samt smak av nötter och choklad. Rostningsprofilen har skapats av den världsberömda danska rostningsmästaren Michael de Renouard.
”Vi valde en mörkrost till fartygets kaffe, vilket passar både finländarnas och svenskarnas nuvarande smakpreferenser gällande rostning. Finländarnas smak gällande kaffe har under de senaste åren utvecklats mot en mörkare rostning. Innan vi gjorde vårt slutgiltiga val testades det nya kaffet i Viking Cinderellas bufférestaurang och personalmässen – och båda testgrupperna gav toppbetyg. Då 8,5 miljoner koppar kaffe bryggs varje år kan inget lämnas åt slumpen!” säger Janne Lindholm.
Viking Lines hållbarhetsmål stannar inte vid produktionskedjan. Kaffesump från fartygen återvinns nämligen som råmaterial för trädgårdsjord. Detta minskar avsevärt användningen av jungfrulig torv vid tillverkningen av mylla.
”Vi har som mål att allt som tagits ombord på fartygen som är möjligt att återvinna ska återanvändas eller återvinnas. Det gäller inte bara kaffet utan även matavfall och till exempel textilier som tas ur bruk. Ett bra exempel på vårt livscykeltänkande är att frityrolja från fartygets restauranger blir till biobränsle för den finska sjöfartsindustrin,” säger Viking Lines hållbarhetschef Dani Lindberg.
Slow Forest Coffee – 5 fakta:
- Slow Forest Coffee är ett kaffeföretag som verkar i Laos, Vietnam och Indonesien i samarbete med över 500 lokala kaffeodlare.
- Företaget grundades år 2019 av Pinja Puustjärvi, driven av en vilja att skydda skogarna i Laos och stötta lokala odlare. Puustjärvi bodde som barn i Laos på grund av sin fars arbete.
- Kaffet odlas i restaurerade kaffeskogar, som binder stora mängder kol och ökar den biologiska mångfalden.
- Det är viktigt för företaget att produktionskedjan är ansvarsfull och transparent, samt att verksamheten gynnar både miljön och de lokala samhällena.
- Slow Forest Coffee betalar odlarna bättre ersättning än genomsnittet i Laos och erbjuder förmåner som underlättar deras liv: förskottsbetalningar, utbildning och möjligheten att låna pengar från en krisfond.
Mera infomation om Slow Forest Coffee här
Tilläggsinformation:
Janne Lindholm, restaurangchef
janne.lindholm@vikingline.com, tel. +358 400 744 806
Dani Lindberg, hållbarhetschef
dani.lindberg@vikingline.com, tel. +358 18 27 000
Johanna Boijer-Svahnström, informationsdirektör
johanna.boijer@vikingline.com, tel. +358 18 270 00
Christa Grönlund, informationschef
christa.gronlund@vikingline.com, tel. +358 9 123 51
Marknadsnyheter
“Vi behöver tillsammans enas om vettiga avtal, som sätter standard för branschen”


Sveriges Radios Kulturnytt gör just nu en mycket välkommen granskning av villkoren i musikbranschen. Igår lyftes artisten Siw Malmkvists situation med ett avtal som inte förnyats på över 60 år. Hennes situation är tyvärr långt ifrån unik. Musikerförbundet har länge uppmärksammat att majorbolagen fortsätter att betala extremt låga royaltynivåer till artister vars kontrakt skrevs på 1960-talet – en tid då digital streaming inte existerade.
– Jag kan intyga att artisterna som talar ut i P1 är långt ifrån ensamma om sin situation och vi uppmanar deras artistkollegor att gå ut med sitt tydliga stöd till de som vågar bryta tystnaden om oskäliga ersättningar, säger Musikerförbundets ordförande Karin Inde.
Musiker och artister skapar det värde som skivbolagen tjänar pengar på, men ändå ser vi gång på gång hur bolagen behåller stora delar av intäkterna. Att en av Sveriges mest folkkära artister, med en karriär som sträcker sig över decennier, fortfarande har en oskälig royalty är ett tydligt bevis på branschens obalans.
– Tystnadskulturen kring prissättning är enbart bra för bolagen. Både artister och musiker skulle verkligen tjäna på att dela med sig till varandra om hur betalningar och dealar verkligen ser ut. Förstås i trygga, egna rum. Det är bara bolagen som tjänar på att vi inte pratar med varandra om pengar, säger Karin Inde.
Stort tack till de modiga artister som ser till att lyfta problematiken! För att vi ska få till en i grunden mer rättvis musikbransch behöver de stora parterna i sammanhanget – skivbolagen, musikerna och artisterna – göra som de flesta andra svenska branscher lyckas med:
– Vi behöver tillsammans enas om vettiga och balanserade avtal, som sätter standard för branschen. Musikerförbundet är redo att göra vår del i arbetet för bättre villkor i musikbranschen, frågan är om skivbolagen är redo, säger Karin Inde.
Karin Inde
Förbundsordförande
karin.inde@musikerforbundet.se
+46 (0)704447228
Musikerförbundet är fackförbundet för professionella musiker och artister. Vi arbetar för förbättrade upphovsrättsliga och arbetsrättsliga villkor och för att våra medlemmar ska få en rättvis del av de värden de skapar i samhället.
-
Analys från DailyFX10 år ago
EUR/USD Flirts with Monthly Close Under 30 Year Trendline
-
Marknadsnyheter5 år ago
BrainCool AB (publ): erhåller bidrag (grant) om 0,9 MSEK från Vinnova för bolagets projekt inom behandling av covid-19 patienter med hög feber
-

 Marknadsnyheter2 år ago
Marknadsnyheter2 år agoUpptäck de bästa verktygen för att analysera Bitcoin!
-
Analys från DailyFX12 år ago
Japanese Yen Breakout or Fakeout? ZAR/JPY May Provide the Answer
-

 Marknadsnyheter2 år ago
Marknadsnyheter2 år agoDärför föredrar svenska spelare att spela via mobiltelefonen
-
Analys från DailyFX12 år ago
Price & Time: Key Levels to Watch in the Aftermath of NFP
-
Analys från DailyFX8 år ago
Gold Prices Falter at Resistance: Is the Bullish Run Finished?
-

 Nyheter7 år ago
Nyheter7 år agoTeknisk analys med Martin Hallström och Nils Brobacke

