Marknadsnyheter
Calquence significantly prolonged the time patients lived without disease progression in relapsed or refractory chronic lymphocytic leukaemia
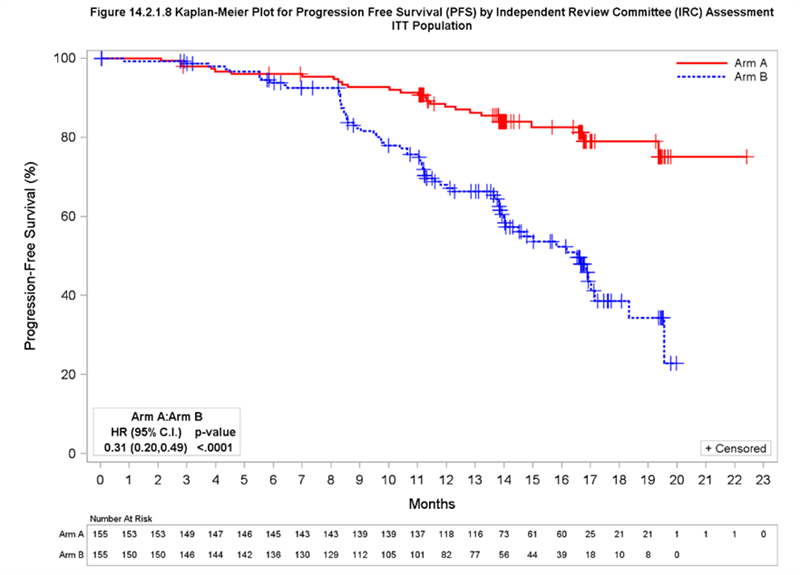
An encouraging 88% of patients on Calquence remained free of disease progression after 12 months, vs. 68% of patients on rituximab combined with idelalisib or bendamustine
AstraZeneca today announced detailed results from the interim analysis of the Phase III ASCEND trial at the European Hematology Association (EHA) Annual Congress in Amsterdam, showing Calquence (acalabrutinib) significantly prolonged the time patients live without disease progression in relapsed or refractory chronic lymphocytic leukaemia (CLL).
The ASCEND trial compared Calquence with the physician’s choice of rituximab combined with idelalisib (IdR) or bendamustine (BR) in patients with relapsed or refractory CLL.
At a median follow-up of 16.1 months, results from the trial showed a statistically-significant and clinically-meaningful improvement in progression-free survival (PFS) for patients treated with Calquence vs. IdR or BR, reducing the risk of disease progression or death by 69% (HR, 0.31; 95% CI, 0.20-0.49, p< 0.0001). The median time without disease progression for patients treated with Calquence has not yet been reached vs. 16.5 months in the control arm. At 12 months, 88% of patients on Calquence showed no disease progression compared to 68% for the control arm. The safety and tolerability of Calquence was consistent with its established profile.
José Baselga, Executive Vice President, Oncology R&D said: “These data add to the growing body of evidence to support the profile of Calquence as a selective BTK inhibitor that offers a chemotherapy-free treatment option with a favourable safety profile in chronic lymphocytic leukaemia, a life-threatening disease. These data, along with our recent positive results from the Phase III ELEVATE-TN trial in previously-untreated chronic lymphocytic leukaemia, will serve as the foundation for regulatory submissions later this year.”
Paolo Ghia, MD, Professor, Medical Oncology, Università Vita-Salute San Raffaele in Milan, and investigator of the ASCEND trial, said: “This is the first randomised trial to directly compare a BTK inhibitor as monotherapy with standard chemoimmunotherapy or idelalisib and rituximab combinations. With a significant improvement in progression-free survival and a favourable safety profile, acalabrutinib may become an important choice for the treatment of patients with relapsed or refractory chronic lymphocytic leukaemia.”
Kaplan-Meier plot for PFS as assessed by an independent review committee in the intent-to-treat population1

Calquence (arm A) vs IdR or BR (arm B)
Safety overview
| Most common (≥15%) AEs, n (%) | Calquence (n=154) |
IdR (n=118) |
BR (n=35) |
|||
| Any | Grade ≥3 | Any | Grade ≥3 | Any | Grade ≥3 | |
| Headache | 34 (22%) | 1 (1%) | 7 (6%) | 0 | 0 | 0 |
| Neutropenia | 30 (19%) | 24 (16%) | 53 (45%) | 47 (40%) | 12 (34%) | 11 (31%) |
| Diarrhoea | 28 (18%) | 2 (1%) | 55 (47%) | 28 (24%) | 5 (14%) | 0 |
| Anaemia | 23 (15%) | 18 (12%) | 11 (9%) | 8 (7%) | 4 (11%) | 3 (9%) |
| Cough | 23 (15%) | 0 | 18 (15%) | 1 (1%) | 2 (6%) | 0 |
| Pyrexia | 19 (12%) | 1 (1%) | 21 (18%) | 8 (7%) | 6 (17%) | 1 (3%) |
| Fatigue | 15 (10%) | 2 (1%) | 10 (8%) | 0 | 8 (23%) | 1(3%) |
| Nausea | 11 (7%) | 0 | 15 (13%) | 1 (1%) | 7 (20%) | 0 |
| IRR | 0 | 0 | 9 (8%) | 2 (2%) | 8 (23%) | 1 (3%) |
| Events of clinical interest for Calquence | ||||||
| Atrial fibrillation | 8 (5%) | 2 (1%) | 4 (3%) | 1 (1%) | 1 (3%) | 1 (3%) |
| Bleeding | 40 (26%) | 3 (2%) | 9 (8%) | 3 (3%) | 2 (6%) | 1(3%) |
| Hypertension | 5 (3%) | 3 (2%) | 5 (4%) | 1 (1%) | 0 | 0 |
| SPM* excluding NMSC** | 10 (6%) | 5 (3%) | 3 (3%) | 0 | 1 (3%) | 1 (3%) |
*Secondary primary malignancy **Non-melanoma skin cancer.
AstraZeneca recently announced that the Phase III ELEVATE-TN trial met its primary endpoint at interim analysis in patients with previously-untreated CLL and that full results will be reported at a forthcoming medical meeting. Calquence is currently approved for the treatment of adults with relapsed or refractory mantle cell lymphoma (MCL) in the US, Brazil, the United Arab Emirates, and Qatar and is being developed for the treatment of CLL and other blood cancers.
About ASCEND
ASCEND (ACE-CL-309) is a global, randomised, multicentre, open-label Phase III trial evaluating the efficacy of Calquence in previously-treated patients with CLL.2 In the trial, 310 patients were randomised (1:1) into two arms. Patients in the first arm received Calquence monotherapy (100mg twice daily until disease progression). Patients in the second arm received physician’s choice of either rituximab in combination with idelalisib or rituximab in combination with bendamustine.1,2
The primary endpoint is PFS assessed by an independent review committee (IRC), and key secondary endpoints include physician-assessed PFS, IRC- and physician-assessed overall response rate (ORR) and duration of response (DoR), as well as overall survival (OS), patient reported outcomes (PROs) and time to next treatment (TTNT).1,2
About Calquence
Calquence (acalabrutinib) was granted accelerated approval by the US Food and Drug Administration (FDA) in October 2017 for the treatment of adult patients with MCL who have received at least one prior therapy. Continued approval for this indication may be contingent upon verification and description of clinical benefit in confirmatory trials.
Calquence is an inhibitor of Bruton tyrosine kinase (BTK). Calquence binds covalently to BTK, thereby inhibiting its activity.3 In B-cells, BTK signalling results in activation of pathways necessary for B-cell proliferation, trafficking, chemotaxis, and adhesion.
As part of an extensive clinical development programme, AstraZeneca and Acerta Pharma are currently evaluating Calquence in 26 company-sponsored clinical trials. Calquence is being developed for the treatment of multiple B-cell blood cancers including CLL, MCL, diffuse large B-cell lymphoma, Waldenstrom macroglobulinaemia, follicular lymphoma, and multiple myeloma and other haematologic malignancies. Beyond the positive Phase III trials ASCEND and ELEVATE-TN, other Phase III trials in CLL are ongoing, including ELEVATE-RR (ACE-CL-006) evaluating acalabrutinib vs. ibrutinib in patients with previously-treated high-risk CLL, and ACE-CL-311 evaluating acalabrutinib in combination with venetoclax and with/without obinutuzumab in patients with previously-untreated CLL without 17p deletion or TP53 mutation.
About chronic lymphocytic leukaemia
Chronic lymphocytic leukaemia (CLL) is the most common type of leukaemia in adults, with an estimated 191,000 new cases globally and 20,720 new cases in the US annually, and prevalence that is expected to grow with improved treatment.4-7 In CLL, too many blood stem cells in the bone marrow become abnormal lymphocytes and these abnormal cells have difficulty fighting infections.4 As the number of abnormal cells grows there is less room for healthy white blood cells, red blood cells and platelets.4 This could result in anaemia, infection and bleeding.4 B-cell receptor signalling through BTK is one of the essential growth pathways for CLL.
About AstraZeneca in haematology
Leveraging its strength in oncology, AstraZeneca has established haematology as one of four key oncology disease areas of focus. The Company’s haematology franchise includes two US FDA-approved medicines and a robust global development programme for a broad portfolio of potential blood cancer treatments. Acerta Pharma serves as AstraZeneca’s haematology research and development arm. AstraZeneca partners with like-minded science-led companies to advance the discovery and development of therapies to address unmet need.
In October 2018, AstraZeneca and Innate Pharma announced a global strategic collaboration that included Innate Pharma licensing the US commercial rights of Lumoxiti (moxetumomab pasudotox-tdfk), and with support from AstraZeneca, will continue EU development and commercialisation, pending regulatory submission and approval.
About AstraZeneca in oncology
AstraZeneca has a deep-rooted heritage in oncology and offers a quickly-growing portfolio of new medicines that has the potential to transform patients’ lives and the Company’s future. With at least six new medicines to be launched between 2014 and 2020, and a broad pipeline of small molecules and biologics in development, we are committed to advance oncology as a key growth driver for AstraZeneca focused on lung, ovarian, breast and blood cancers. In addition to our core capabilities, we actively pursue innovative partnerships and investments that accelerate the delivery of our strategy as illustrated by our investment in Acerta Pharma in haematology.
By harnessing the power of four scientific platforms – Immuno-Oncology, Tumour Drivers and Resistance, DNA Damage Response and Antibody Drug Conjugates – and by championing the development of personalised combinations, AstraZeneca has the vision to redefine cancer treatment and one day eliminate cancer as a cause of death.
About AstraZeneca
AstraZeneca is a global, science-led biopharmaceutical company that focuses on the discovery, development and commercialisation of prescription medicines, primarily for the treatment of diseases in three therapy areas – Oncology, Cardiovascular, Renal & Metabolism and Respiratory. AstraZeneca operates in over 100 countries and its innovative medicines are used by millions of patients worldwide. For more information, please visit www.astrazeneca.com and follow us on Twitter @AstraZeneca.
| Media Relations | ||
| Gonzalo Viña | +44 203 749 5916 | |
| Rob Skelding | Oncology | +44 203 749 5821 |
| Rebecca Einhorn | Oncology | +1 301 518 4122 |
| Matt Kent | BioPharma | +44 203 749 5906 |
| Jennifer Hursit | Other | +44 203 749 5762 |
| Christina Malmberg Hägerstrand | Sweden | +46 8 552 53 106 |
| Michele Meixell | US | +1 302 885 2677 |
| Investor Relations | ||
| Thomas Kudsk Larsen | +44 203 749 5712 | |
| Henry Wheeler | Oncology | +44 203 749 5797 |
| Christer Gruvris | BioPharma (cardiovascular; metabolism) | +44 203 749 5711 |
| Nick Stone | BioPharma (respiratory; renal) | +44 203 749 5716 |
| Josie Afolabi | Other medicines | +44 203 749 5631 |
| Craig Marks | Finance, fixed income | +44 7881 615 764 |
| Jennifer Kretzmann | Corporate access, retail investors | +44 203 749 5824 |
| US toll-free | +1 866 381 72 77 |
References
1 Ghia P, Pluta A, Wach M, et al. ASCEND Phase 3 study of acalabrutinib vs. investigator’s choice of rituxumab plus idelalisib (idR) or bendamustine (BR) in patients with relapsed/refractory chronic lymphocytic leukaemia (CLL). Abstract LB2606 at: European Hematology Association 2019 Annual Meeting. Available online. Accessed June 2019.
2 ClinicalTrials.gov. A Study of Acalabrutinib vs Investigator’s Choice of Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in R/R CLL. NCT02970318. Available online. Accessed June 2019.
3 CALQUENCE® (acalabrutinib) Prescribing Information. AstraZeneca Pharmaceuticals LP, Wilmington, DE.
4 National Cancer Institute. Chronic Lymphocytic Leukaemia Treatment (PDQ®)–Patient Version. Available online. Accessed June 2019.5Global Burden of Disease Cancer Collaboration. JAMA Oncol. 2017;3(4):524-528.
5 Global Burden of Disease Cancer Collaboration. JAMA Oncol. 2017;3(4):524-52.
6 National Institute of Health SEER Program. Cancer Stat Facts: Leukemia—Chronic Lymphocytic Leukemia (CLL). Available online. Accessed June 2019.
7 Jain N, et al. Prevalence and Economic Burden of Chronic Lymphocytic Leukemia (CLL) in the Era of Oral Targeted Therapies. Blood. 2015;126:871.
Marknadsnyheter
ZINZINO AB (PUBL): Zinzino förvärvar inkråm i Xeliss – strategisk förstärkning i södra Europa och inom mikroalgen spirulina
Zinzino, det globala varumärket för hälsa och välmående från Skandinavien, har via ett inkråmsförvärv övertagit rättigheterna till det luxemburgsbaserade direktförsäljningsbolaget Xellis distributörsdatabas och tillhörande kundregister, varulager och IP-rättigheter. Detta är ytterligare ett strategiskt viktigt steg i Zinzinos tillväxtplaner med fokus på att förbättra personlig hälsa och välbefinnande på global nivå med nyskapande bioteknik och en banbrytande produktportfölj som marknadsförs genom direktförsäljning.
Xelliss är ett globalt direktförsäljningsföretag med bas i Luxenburg. Varumärkesportföljen erbjuder en rad naturliga och innovativa produkter inom välbefinnande, näring och kosmetika, baserade på mikroalgen spirulina från egen produktion.
Ett visionärt tänkesätt, tech first-perspektiv, testbaserad kost med näring på cellnivå samt en stark position för att dra nytta av nuvarande trender kommer att forma grunden för partnerskapet med Xellis. Sedan förvärvet av VMA Life 2020, Enhanzz 2022 och det strategiska samarbetet med ACN under ingången av 2024 har Zinzino letat efter ytterligare kraftfulla investeringar för att behålla sin hållbara, lönsamma tillväxt, stärka sin distributionskraft, expandera till nya marknader och utnyttja produktportföljen inom nya konsumentområden.
– Individuell rådgivining och skräddarsydda lösningar är framtiden, och inte bara inom hälsa och friskvård, säger Dag Bergheim Pettersen, VD på Zinzino och Jean-Michel Larré, VD och grundare Xellis. Tillsammans har vi mångårig kombinerad branscherfarenhet och allt som krävs för att driva den moderna, personliga shoppingupplevelsen genom direktförsäljning.
Zinzino förvärvar Xelliss distributörsorganisation samt varulager och IP-rättigheter till produktlinjerna. Verksamheten som under föregående år omsatt ca 8 mEUR förväntas kunna skapa stark tillväxt genom de synergier som uppstår i de gemensamma nätverken. Bruttomarginalerna i verksamheten är goda och lönsamheten kommer därmed kunna utvecklas mycket väl genom utnyttjande av ZInzinoz befintlliga tekniska plattform och organisation.
Zinzino skall vid tillträdet betala en fast köpeskilling om 2 mEUR fördelat på 50% kontant och 50% nyemitterade Zinzino-aktier. Dessutom tillkommer villkorade tilläggsköpeskillingar baserat på försäljningsutvecklingen genererat av den förvärvade distributörsorganisationen under perioden 2024–2029. De totala tilläggsköpeskillingarna beräknas uppgå till 4,0 mEUR men kan vid maximalt utfall uppgå till 8,0mEUR och skall till 100% regleras med nyemitterade Zinzino-aktier. Den kontanta delen av köpeskillingen finansieras med egen kassa.
För mer information, vänligen kontakta:
Dag Bergheim Pettersen CEO Zinzino +47 (0) 932 25 700, zinzino.com
Fredrik Nielsen CFO Zinzino +46 707 900 174, fredrik.nielsen@zinzino.com
Bilder för fri publicering:
marketing@zinzino.com
Certified Adviser: Carnegie Investment Bank AB (publ)
Denna information är sådan som Zinzino AB (publ) är skyldig att offentliggöra enligt EU:s marknadsmissbruksförordning. Informationen lämnades genom ovanstående kontaktpersons försorg för offentliggörande kl. 13.00 den 12 maj 2024.
Zinzino är ett globalt direktförsäljningsföretag från Skandinavien som specialiserat sig på testbaserade, personligt anpassade kosttillskott och vetenskaplig hudvård. Det är ett aktiebolag med aktier noterade på Nasdaq First North Premier Growth Market. Företagets vetenskapligt beprövade kosttillskott finns på mer än 100 marknader över hela världen. Zinzino äger det schweiziska biotekniska hudvårdsvarumärket HANZZ+HEIDII samt de norska forsknings- och produktionsenheterna BioActive Foods AS och Faun Pharma AS. Företagets huvudkontor ligger i Sverige, i Göteborg, med ytterligare kontor i Europa, Asien, USA och Australien.
Taggar:
Marknadsnyheter
Yoga: Positiva effekter i rättspsykiatrin
En ny studie visar att yoga kan ha betydande fördelar för intagna individer med
allvarliga psykiatriska störningar. Genom att implementera traumafokuserad yoga
observerades minskningar av negativa emotionella tillstånd, ångest och fientlighet
hos deltagarna. Dessa positiva effekter sågs inte hos dem som ägnade sig åt andra
former av fysisk aktivitet. Resultaten, publicerade i Psychiatry Research, markerar ett
genombrott för användningen av yoga som kompletterande vårdintervention inom
rättspsykiatrin. Ett strukturerat yoga-program och utbildning för vårdpersonal har
utvecklats och visat sig vara genomförbart och gynnsamt för patienternas
välmående.
Marknadsnyheter
Civilministern reser vidare – besöker Värmland
Måndag den 13 maj fortsätter civilminister Erik Slottner sin resa genom Sverige med att under tre dagar besöka Årjäng, Karlstad och Kristinehamn.
I Årjäng besöker Erik Slottner under måndagen kommunhuset och Nordmarkens destilleri. Civilministern bjuder därefter in till en AW på Krogeriet i Årjäng dit allmänhet och media är välkomna för samtal och frågor.
Under tisdagen går resan vidare till Karlstad där civilministern besöker Nobelgymnasiet och träffar företrädare från kommunen för samtal om bland annat innovation och digital utveckling. Statsrådet åker därefter vidare till Karlstad universitet för samtal om bland annat universitetets styrkor och utmaningar samt AI.
Tisdagen avslutas sedan med en AW på Bishop Arms i Karlstad för samtal om det kommande EU-valet. Allmänhet och media är välkomna att ställa frågor.
Under onsdagen besöker civilminister Erik Slottner Kristinehamns kommun för samtal om bland annat digitalisering och utmaningar inom välfärdstjänster.
För mer information eller intervjuförfrågningar kontakta Samuel Dalevi.
Presskontakt:
Samuel Dalevi
Pressekreterare hos civilminister Erik Slottner
Tel 076 133 51 18
samuel.dalevi@regeringskansliet.se
Taggar:
-
Analys från DailyFX8 år ago
EUR/USD Flirts with Monthly Close Under 30 Year Trendline
-

 Marknadsnyheter1 år ago
Marknadsnyheter1 år agoUpptäck de bästa verktygen för att analysera Bitcoin!
-
Marknadsnyheter4 år ago
BrainCool AB (publ): erhåller bidrag (grant) om 0,9 MSEK från Vinnova för bolagets projekt inom behandling av covid-19 patienter med hög feber
-
Analys från DailyFX11 år ago
Japanese Yen Breakout or Fakeout? ZAR/JPY May Provide the Answer
-
Analys från DailyFX11 år ago
Price & Time: Key Levels to Watch in the Aftermath of NFP
-
Analys från DailyFX7 år ago
Gold Prices Falter at Resistance: Is the Bullish Run Finished?
-

 Nyheter5 år ago
Nyheter5 år agoTeknisk analys med Martin Hallström och Nils Brobacke
-
Marknadsnyheter6 år ago
Tudorza reduces exacerbations and demonstrates cardiovascular safety in COPD patients

